Etudier expérimentalement et numériquement les écoulements transvalvulaires aortiques dans le cadre du TAVI
Publié par Guillaume Oger, le 12 décembre 2025 460
Les maladies cardiovasculaires sont l’une des deux principales causes de mortalité en Occident. Parmi les cardiopathies responsables, les valvulopathies notamment aortiques constituent une cause majeure chez le patient âgé. Le remplacement valvulaire aortique percutané (sans ouverture sternale, sans circulation extra-corporelle) est devenu en 15 ans un traitement de référence. Initialement réservé aux patients contre-indiqués à la chirurgie classique, le TAVI (Transcatheter Aortic Valve Implantation) est devenu un traitement de première intention chez les patients à risque intermédiaire, voire à bas risque. Cette évolution vers le bas risque et chez des sujets plus jeunes impose d’implanter au patient la valve la plus respectueuse de l’hémodynamique cardiaque et la plus adaptée à son anatomie. Si le choix de la famille de valves est guidé entre autres par l’anatomie valvulaire et son niveau de calcification, ce choix est très largement guidé par les habitudes du praticien.
Unissant le CHU-Nantes, le LHEEA de l’Ecole Centrale Nantes et I2M Bordeaux, le projet ANR « AorticVirtu_et_al » s’est intéressé à l’élaboration d’outils à la fois expérimentaux et numériques pour tenter de prédire, avec une précision accrue, l’hémodynamique transvalvulaire aortique après TAVI. Ces travaux ont également bénéficié du soutien de la Région Pays de Loire (Trajectoire nationale de la recherche ligérienne) et du groupement GliCID (Groupement Ligérien pour le Calcul Intensif Distribué https://www.glicid.fr/ ).
Elaboration d’un banc vasculaire expérimental
Un banc vasculaire visant à reproduire expérimentalement l’écoulement à travers une bioprothèse de valve aortique a été développé au sein du LHEEA de l’Ecole Centrale Nantes. Ce banc d’essai, toujours en cours de perfectionnement, permettra bientôt de fournir des données indépendantes visant à renforcer les connaissances sur la dynamique de couplage entre les déformations des feuillets de la valve et les caractéristiques de l’écoulement pulsé la traversant, notamment les champs de pression et de vitesse en amont et en aval. Ce prototype est constitué d’une pompe imitant le fonctionnement d’un ventricule gauche, propulsant un mélange eau-glycérine approchant la densité et la viscosité du sang humain.
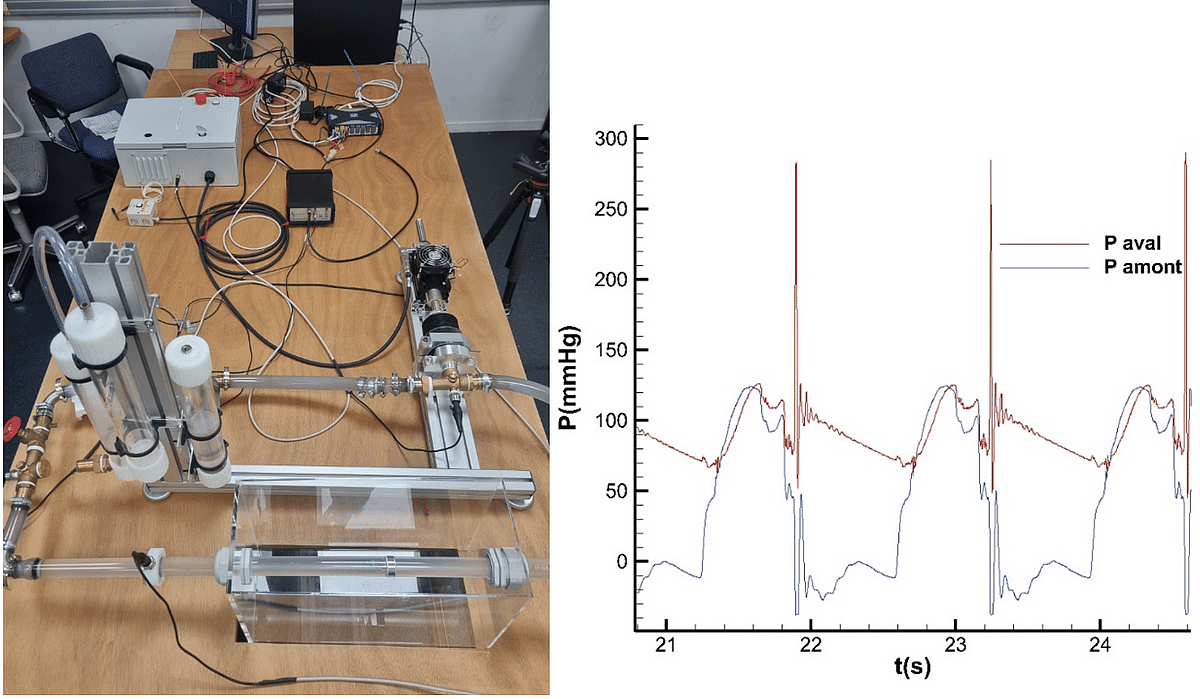
Figure 1: Photo en vue de dessus du banc vasculaire (à gauche). Exemple de signaux de pression mesurés sur le banc vasculaire en amont et en aval de la valve, approchant les caractéristiques physiologiques attendues chez un patient humain (à droite).
Ce « ventricule » alimente une « aorte » faite d’un tube en acrylique dans laquelle les praticiens du CHU de Nantes ont préalablement implanté une valve bioprothétique.
Ce banc d’essai permet d’observer, à l’aide d’une caméra rapide, la dynamique de la bio-prothèse lorsqu’elle est soumise à l’écoulement pulsé, et à mesurer les profils de vitesse via un dispositif de Vélocimétrie Doppler à Ultrasons (UDV). Ces enregistrements sont ensuite analysés afin de caractériser différentes phases d’ouverture et de fermeture de la valve, pour différents régimes hémodynamiques.
Figure 2: Valve aortique au sein de sa veine d’essai (à droite) ; électrode UDV et son gel de transmission échographique (à gauche).
Elaboration d’un banc vasculaire numérique
Depuis septembre 2022, un projet doctoral dans le cadre du projet ANR « AorticVirtu_et_al » a permis de développer des outils numériques permettant de simuler l’Interaction Fluide-Structure spécifiquement dans le cas d’un écoulement pulsé au travers de la valve aortique [4]. Le premier axe de recherche se focalise sur le couplage entre la méthode Lattice-Boltzmann (LBM), pour la partie fluide, et la méthode Eléments-Finis (FEM) pour la partie solide [2][3]. Les premiers travaux de recherche ont eu pour objectif de consolider les données préliminaires déjà obtenues afin de mieux appréhender la dynamique de la valve sous écoulement pulsé.
Le développement de ce nouveau modèle de couplage fluide-structure a nécessité une phase de validation sur des cas-test simplifiés, dont le comportement présente des similarités avec les feuillets de la valve aortique [2]. Le cas-test dit « Flapping flag » -un drapeau qui flotte au vent- a été choisi notamment car le drapeau et les feuillets de la bio-prothèse sont des structures minces présentant un mouvement caractéristique de battement. Dans ce cas-test, la structure mince du drapeau est soumise à un écoulement constant et uniforme de 1 m/s. Sous l’effet de cet écoulement, le drapeau oscille et « bat » à une certaine fréquence théorique attendue.
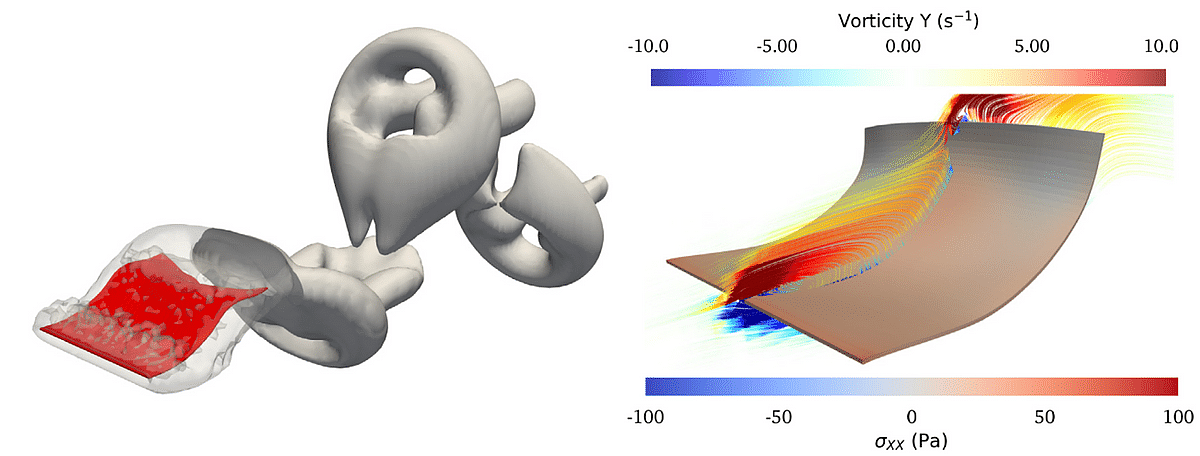
Figure 3 : Cas test dit de “Flapping-flag” à Reynolds 200: structures tourbillonnaires (à gauche) ; champs de vorticité et de contrainte axiale dans le drapeau (à droite) [3].
Le fluide simulé ici via la méthode Lattice Boltzmann utilise une grille fixe composée d’environ 18 millions de nœuds. La structure du drapeau (Eléments Finis) comporte environ 27200 nœuds. La taille importante de ce cas-test a nécessité la parallélisation de nos solveurs LBM et FEM, c’est-à-dire une distribution du calcul sur un réseau de processeurs afin d’accélérer les simulations et de diminuer les temps de calculs. Au total, 99 processeurs ont été nécessaires à la réalisation de cette simulation, lancée sur le supercalculateur de GLiCID (Groupement Ligérien pour le Calcul Intensif Distribué https://www.glicid.fr/ ).
Ces résultats préliminaires ont permis de réaliser nos premières simulations d’écoulements transvalvulaires aortiques, en réponse à un débit instantané physiologique imposé [3], comme illustré dans la figure ci-dessous.
Figure 4: Haut : exemple de courbe de débit instantané imposé en amont de la valve aortique. Milieu : réponse obtenue en simulation numérique couplée fluide-structure pour cet écoulement transvalvulaire aortique par couplage LBM-FEM sur une géométrie aortique test [1][3] (contour correspondant au champ de vitesse axiale dans différents plans de coupe à l’instant t= 0.55 s). Bas : déformations calculées pour les feuillets de valves à différents instants de son ouverture.
Perspectives
La suite de ces travaux portera notamment sur la mise en œuvre de la vélocimétrie par imagerie de particules (PIV) au sein du banc expérimental, afin d'obtenir des cartographies 2D détaillées du champ de vitesse dans le jet aortique, et d’effectuer la validation des outils numériques LBM-FEM développés pendant le projet ANR « AorticVirtu_et_al ». Le banc d'essai sera également amélioré par l'intégration d'une anatomie réaliste des sinus de Valsalva, permettant une meilleure reproduction des phénomènes de vortex et des zones de recirculation associés à la fermeture valvulaire. Enfin, une comparaison systématique entre différentes bioprothèses aortiques sera menée, combinant des approches expérimentales et numériques (interaction fluide-structure basée sur la méthode LBM-FEM), afin de valider les modèles in silico et d'identifier les dispositifs offrant les meilleures performances hémodynamiques, évaluées à partir de biomarqueurs classiquement adoptés tels que le cisaillement pariétal et l’ouverture effective de valve.
Références
[1] J. Sigüenza, D. Pott, S. Mendez, S.J. Sonntag, T.A. Kaufmann, U. Steinseifer, F. Nicoud, Fluid‐structure interaction of a pulsatile flow with an aortic valve model: A combined experimental and numerical study. International journal for numerical methods in biomedical engineering, Volume 34, 2018.
[2] Z. Li, G. Oger, D. Le Touzé, A partitioned framework for coupling LBM and FEM through an implicit IBM allowing non-conforming time-steps: Application to fluid-structure interaction in biomechanics. Journal of Computational Physics, Volume 449, 2022.
[3] J. Lopez, Z. Li, G. Oger, An LBM-FEM robust and efficient fluid–structure coupling scheme for partitioned numerical simulation of blood flow-aortic valve interaction. Computers in Biology and Medicine, Volume 196, 2025.
[4] Jolan Lopez, Simulation of transaortic flows using Smoothed Particle Hydrodynamics and Lattice Boltzmann methods coupled with Finite Element method - Application to personalized virtual transcatheter aortic valve assessment, PhD Thesis, Ecole Centrale de Nantes, France, 2025.

