Une arthrose, des arthroses : repenser la maladie pour mieux la traiter
Publié par Nantes Université, le 22 avril 2026 350
L’arthrose est la maladie articulaire la plus répandue dans le monde. Elle se caractérise par une dégradation du cartilage, une altération de l’os et une inflammation de la membrane synoviale. Cette membrane synoviale est une fine couche de tissu qui tapisse l’intérieur de l’articulation jouant un rôle clé dans sa protection et sa lubrification, et dont l’inflammation provoque des douleurs et une diminution de la mobilité chez le patient. De nombreux facteurs peuvent être à l'origine de son apparition, qu'il s'agisse de facteurs environnementaux, comme l'alimentation, le manque d’activité physique ou la sédentarité, ou biologiques, comme la génétique ou le surpoids.
Même s'il existe des traitements visant à soulager la douleur, aucun traitement curatif n'est actuellement disponible. L’arthrose présente de nombreuses variabilités d'un individu à l'autre aussi bien au niveau des symptômes que des processus intrinsèques induisant la maladie, ce qui peut représenter un obstacle majeur au développement d'un traitement. Certaines mesures sont toutefois recommandées pour ralentir la progression de la maladie, comme la pratique d'une activité physique modérée ou la perte de poids.
Comment vraiment caractériser l’arthrose ?
Le diagnostic de l’arthrose repose sur plusieurs observations de l’articulation. Une radiographie de l’articulation permet d’observer les tissus calcifiés comme les os. Leur rapprochement est un signe indirect de l’usure du cartilage, qui s’amincit progressivement au cours de l’arthrose. Cette image permet ainsi de détecter les atteintes articulaires et permet au clinicien d'évaluer la présence ou l'absence d'arthrose ainsi que sa sévérité, le cas échéant. Des examens par échographie, IRM ou arthroscopie peuvent fournir des informations supplémentaires sur l’état de l’articulation, comme la présence d’une inflammation de la membrane synoviale, ainsi que de fissures et d’un amincissement de la surface du cartilage.
L’observation histologique des tissus articulaires au microscope permet de mieux comprendre les mécanismes de l’arthrose et en révèle la complexité. À partir de fragments de tissus, appelés explants, les chercheurs analysent en détail les modifications qui affectent les différentes structures de l’articulation.
Au niveau du cartilage, ces analyses révèlent une altération progressive de son organisation. La matrice qui lui confère ses propriétés mécaniques se dégrade, certaines cellules deviennent anormalement volumineuses ou se regroupent en amas, et la surface du cartilage s’érode. Parallèlement, l’os situé sous le cartilage subit également des remaniements, mis en évidence grâce à des techniques de coloration des tissus. L’ensemble de ces altérations peut être évalué à l’aide du score OARSI, un outil utilisé pour mesurer le degré de dégradation du cartilage.
La membrane synoviale est elle aussi fortement impliquée dans l’arthrose. Ce tissu subit un épaississement lié à l’inflammation. Elle est constituée de deux couches : une couche interne, directement en contact avec l’articulation qui peut s’épaissir, et une couche plus profonde, composée principalement de cellules de soutien. Les observations histologiques montrent une augmentation du nombre de cellules immunitaires dans la couche interne. L’intensité de cette inflammation varie selon les patients. Elle peut être évaluée grâce au score de Krenn, qui prend en compte plusieurs critères, dont l’épaisseur de la couche interne et la densité de cellules composant cette membrane.
Une observation plus poussée de la membrane synoviale a permis de déchiffrer plus précisément la composition de cette inflammation et ainsi de définir trois profils inflammatoires, ou histopathotypes : le profil pauci-immun (PI), le profil myéloïde-diffus (DM) et le profil lympho-myéloïde (LM). Le profil PI est caractérisé par une faible présence de cellules immunitaires et une fibrose avancée dans la sous-intima, le profil DM par la présence principalement de macrophages, des cellules permettant d’éliminer certains débris cellulaires de l’organisme et régulant l’inflammation et enfin le profil LM, caractérisé par la présence de nombreuses cellules immunitaires comme des macrophages mais également des lymphocytes, des cellules du système immunitaire spécialisées dans la reconnaissance et la défense ciblée contre les agents étrangers, comme les virus ou certaines bactéries, se regroupant en périphérie des vaisseaux sanguins sous la forme d’amas cellulaires appelés structures lymphoïdes ectopiques (ELS). Ces histopathotypes ont pu être mis en lien avec certaines données cliniques, reflétant notamment l’inflammation de bas grade observée dans le sang des patients atteints d'arthrose. Les travaux réalisés dans notre laboratoire visent ainsi à mieux stratifier les patients arthrosiques, c’est-à-dire à les répartir en sous-groupes selon les caractéristiques de leur maladie. Ces sous-groupes ont permis de considérer qu’il existe plusieurs arthroses différentes avec des manifestations articulaires variées, ouvrant la voie à la médecine personnalisée pour le traitement de ces maladies : un type d'arthrose, un médicament adapté.
L’inflammation, un acteur central dans le développement de l’arthrose !
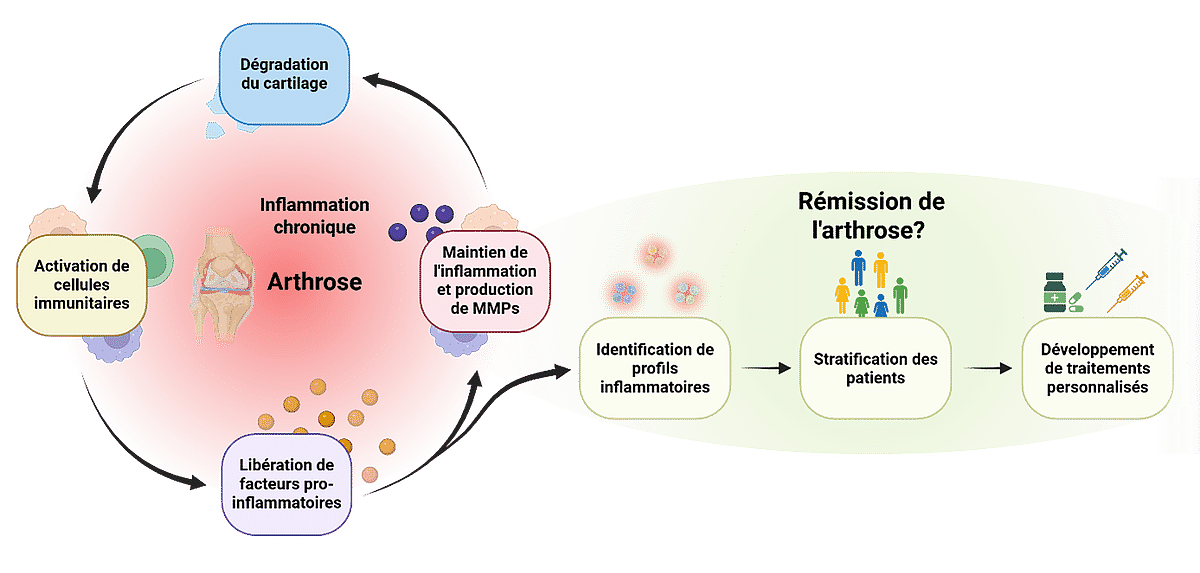
L’inflammation est de plus en plus reconnue comme étant impliquée dans le développement et la progression de l’arthrose. De nombreuses études ont permis d'étudier divers processus inflammatoires dans le contexte arthrosique, et ont ainsi apporté un éclairage nouveau sur ces pathologies. Au cours de la maladie, des débris cartilagineux sont présents dans le liquide synovial, le fluide qui lubrifie et nourrit l’articulation. Ces débris sont perçus par l’organisme comme des signaux de danger et stimulent les cellules immunitaires présentes en conditions physiologiques, c’est-à-dire à l’état normal de fonctionnement et d’équilibre de l’organisme. Leur présence active donc une réponse inflammatoire et provoque la production de métalloprotéinases (MMPs), des protéines capables de dégrader le cartilage. L’accumulation de débris cartilagineux en résultant entretient un cercle vicieux, où la destruction du cartilage favorise une inflammation chronique de l’articulation.
L’inflammation de la membrane synoviale a déjà été reconnue comme un facteur en lien avec la douleur ressentie par les patients arthrosiques. Son rôle dans le développement de la maladie fait actuellement l'objet de nombreux travaux de recherche.
Les avancées récentes ont permis de mettre en évidence une grande diversité de cellules inflammatoires dans le tissu synovial inflammé dans le contexte arthrosique, en particulier au sein des macrophages, dont les fonctions apparaissent multiples et spécialisées.
Ces avancées révèlent également un déséquilibre entre les différentes populations cellulaires : les cellules aux propriétés anti-inflammatoires sont globalement moins nombreuses tandis que les cellules pro-inflammatoires sont davantage présentes dans la membrane synoviale arthrosique que dans un tissu sain. Par ailleurs, le rôle des amas de lymphocytes observés chez les patients présentant un profil inflammatoire LM reste encore mal compris. Certaines données suggèrent qu’elles pourraient être activées et impliquées dans des mécanismes de type auto-immuns sans que cela n’ait pu être clairement démontré. Des études sont actuellement en cours pour mieux comprendre le rôle de ces amas, notamment en analysant la diversité des lymphocytes les composant, ainsi que leur état d’activation, afin d’évaluer une possible composante auto-immune dans l’arthrose.
L’observation de différents profils inflammatoires dans les tissus arthrosiques suggère que l’arthrose ne repose pas sur un seul mécanisme inflammatoire, mais sur plusieurs, qui varient selon les patients. Il apparaît donc important de mieux comprendre comment ces mécanismes moléculaires, ou endotypes, diffèrent d’un individu à l’autre, en lien avec les histopathotypes décrits précédemment.
Moduler les populations macrophagiques, le futur du traitement de l’arthrose ?
Comme mentionné en introduction, les traitements médicamenteux, tels que les AINS ou les corticoïdes, visent uniquement à soulager la douleur. Aucun traitement universel n’existe à ce jour, en raison de l’existence de plusieurs types d’arthrose. Il est aujourd’hui établi que l’arthrose ne repose pas sur un seul mécanisme biologique, mais sur une diversité de processus moléculaires qui diffèrent d’un patient à l’autre. Cette hétérogénéité est aujourd’hui considérée comme l’une des principales raisons pour lesquelles de nombreux traitements ont échoué : une même thérapie ne peut pas fonctionner chez deux patients dont les tissus articulaires présentent des profils inflammatoires distincts. Il devient donc essentiel de mieux classer les patients selon ces caractéristiques, puis d’identifier des cibles thérapeutiques spécifiques à chaque endotype afin de développer des traitements personnalisés mieux adaptés à chacun. C’est précisément sur cet aspect que nous avons concentré nos travaux au sein de notre laboratoire.
L’identification de sous-populations de macrophages associées à chaque pathotype, à laquelle nos travaux ont contribué, pourrait ouvrir la voie à des traitements plus ciblés. Comme ces cellules immunitaires n’exercent pas les mêmes fonctions selon les histopathotypes, il serait possible de moduler leur activité de manière spécifique chez chaque patient afin de réduire l’inflammation. En ciblant précisément ces macrophages en fonction de l’histopathotype, il serait possible de limiter l’inflammation de la membrane synoviale et favoriser progressivement le rétablissement de l’équilibre biologique (homéostasie) au sein de l’articulation.
Plusieurs défis restent néanmoins à relever, mais ils s’inscrivent dans une dynamique de recherche prometteuse. Des sous-populations macrophagiques impliquées dans l’arthrose ont déjà été identifiées, ce qui constitue une avancée majeure vers des thérapies ciblées ; les études futures permettront de déterminer si leur modulation peut restaurer l’équilibre biologique dans l’articulation. Par ailleurs, l’établissement des pathotypes repose sur une biopsie de la membrane synoviale, c’est-à-dire le prélèvement d’un petit fragment de tissu destiné à être analysé en laboratoire. Bien que cette procédure soit jugée simple et peu traumatique pour le patient, elle n’est pas encore réalisée en routine clinique.
En définitive, la stratification des patients apparaît comme un tournant majeur dans la prise en charge de l’arthrose. Les progrès réalisés dans l’identification des histopathotypes et des mécanismes moléculaires sous-jacents ouvrent des perspectives prometteuses pour le développement de traitements personnalisés, mieux adaptés aux besoins de chaque patient.
Article rédigé par Nicolas GAIGEARD, doctorant en 3ème année, au sein du laboratoire Inserm/Nantes Université/Oniris UMR 1229-RMeS (Regenerative Medicine and Skeleton), sous la co-direction de Marie-Astrid BOUTET et Jérôme GUICHEUX. La thèse a été réalisée grâce à une allocation doctorale cofinancée par la Région Pays de la Loire et l’Inserm
Photo de couverture par CHUTTERSNAP (@chuttersnap) sur Unsplash