Le fluor, l’ennemi qui vous veut du bien
Publié par Edouard Boivin, le 7 octobre 2025 1.4k
Bien que les polluants éternels (les PFAS = Substances Per- et PolyFluoroAlkylées) contiennent du fluor, attribuer à ce dernier la responsabilité de cette crise sanitaire et environnementale reviendrait à accuser le carbone ou l’oxygène d’être à l’origine de celle liée au dioxyde de carbone (CO2). Pourtant, le carbone et l’oxygène sont des éléments essentiels à la vie, tout comme le fluor, dont les propriétés si singulières en font un acteur clé de la transition énergétique, des nouvelles technologies et du domaine de la santé. Dans l’opinion publique, dans certains médias, voire même dans le milieu académique, l’amalgame entre composés fluorés et PFAS reste malheureusement courant. Or, si les PFAS sont bien des composés fluorés, la réciproque n’est pas nécessairement vraie. Dans cet article, après avoir rappelé les grandes lignes de la problématique relative aux PFAS, nous examinerons l’application des composés fluorés - ne relevant pas de la catégorie des PFAS - dans divers domaines actuels et futurs.
Le très préoccupant cas des PFAS
Les PFAS sont une vaste famille de plus 4000 composés chimiques synthétiques utilisés depuis les années 1950. Ils se caractérisent par une résistance exceptionnelle à la chaleur, à l’eau, aux ultraviolets et à de nombreux agents chimiques. C’est cette particularité qui leur a valu le surnom de “polluants éternels”, car ils se dégradent très lentement dans l’environnement. On les retrouve dans une multitude de produits du quotidien : poêles antiadhésives, emballages alimentaires imperméables, textiles déperlants, mousses anti-incendie, cosmétiques, équipements médicaux ou encore revêtements de panneaux solaires ou de pales d’éolienne. Si leur résistance a largement favorisé leur essor dans l’industrie et envahi notre quotidien, cette persistance soulève aujourd’hui de graves problèmes sanitaires et environnementaux. Ils s’accumulent dans l’eau, les sols et les organismes vivants, y compris l’être humain. Ils sont détectés aujourd’hui partout dans le monde, même dans des zones éloignées de toute activité industrielle. Leurs effets sur la santé suscitent une vive inquiétude : des études scientifiques relient l’exposition prolongée aux PFAS à des troubles hormonaux, à une diminution de la fertilité, à des perturbations du système immunitaire, à un risque accru de certains cancers, ainsi qu’à des effets sur le développement des enfants. Sur le plan environnemental, leur dissémination contamine les nappes phréatiques, les rivières et les chaînes alimentaires. Ils représentent ainsi une menace pour la biodiversité aquatique et terrestre, s’accumulant dans les poissons et autres animaux sauvages, puis remontant jusqu’à l’homme via l’alimentation. Face à ces dangers, plusieurs pays européens et organismes internationaux militent pour restreindre, voire interdire, certains PFAS. Cependant, pour certaines de ces applications, leur substitution reste complexe, tant leurs propriétés sont difficiles à remplacer. Ainsi, les PFAS illustrent parfaitement le dilemme entre innovation - parfois au service de l’écologie ou de la santé - et conséquences sanitaires et écologiques de leur exploitation. Leur gestion constitue aujourd’hui un défi majeur de santé publique et de protection de l’environnement.
Fluor et santé
En santé humaine, l’usage le plus connu du fluor, sous sa forme d’ion fluorure F-, est sans nul doute pour la prévention des caries dentaires ; il s’intègre dans l’émail des dents pour former la fluorapatite, Ca5(PO4)3F, un composé résistant aux attaques acides. Outre les dentifrices, il est également ajouté dans les bains de bouche et, dans certains pays, directement dans l’eau potable. Cette dernière pratique reste contestée (notamment par l’administration américaine actuelle), mais selon les Centers for Disease Control (l’équivalent américain de santé publique France), la fluoration de l’eau figure parmi les dix plus grands succès de santé publique du 20ᵉ siècle, aux côtés de la vaccination, de la lutte contre le tabagisme ou encore du contrôle des maladies infectieuses. L’OMS classe d’ailleurs le fluor parmi les 14 éléments chimiques essentiels à la santé. En effet, son usage ne se limite pas aux dentifrices puisqu’il est présent dans près de 340 médicaments, soit environ 1 sur 5 ! On le retrouve ainsi dans des traitements contre des maladies de peau, des infections, des cancers, des virus ou encore des troubles de la circulation sanguine. S’il est autant présent dans nos pharmacies, c’est pour trois raisons principales :
- La liaison entre le carbone et le fluor est très solide, ce qui prolonge la durée d’action du médicament dans le corps,
- les molécules fluorées, attirées par les graisses, traversent plus facilement la membrane des cellules pour mieux atteindre leur cible,
- l’ajout de fluor peut changer profondément les propriétés chimiques d’une molécule, ce qui améliore sa sélectivité et son efficacité.
Le fluor occupe également une place de choix dans l’imagerie médicale, notamment en TEP (Tomographie par Emission de Positons) grâce à un isotope du fluor, le fluor-18 (¹⁸F), produit dans un cyclotron, comme celui du centre Arronax près de Nantes. Le fluor-18, relativement instable, avec une période radioactive de 2 heures environ, est combiné à un dérivé du glucose qui se fixe aux cellules cancéreuses, permettant ainsi de les visualiser sur les images TEP.
Fluor et nouvelles technologies
Dans les télécommunications, le fluor est un acteur discret mais tout aussi indispensable. Il est ajouté aux verres de silice pour fabriquer les fibres optiques, ce qui améliore la transmission de la lumière. Résultat : l’information circule à grande vitesse et sans perte sur des milliers de kilomètres, rendant possible l’essor d’internet et des réseaux mondiaux. En électronique, le fluor a aussi une place clé : des composés fluorés tel que SF6, sous forme gazeuse, servent à graver les semi-conducteurs lors de la fabrication des puces, cœur de tous nos appareils numériques. Le fluor est également un élément central dans la production industriel de l’aluminium par électrolyse (65 Mt en 2020), grâce à la cryolite (Na3AlF6). Ce métal, à la fois léger, solide et recyclable à l’infini, est omniprésent dans l’aéronautique, le spatial ou encore l’automobile. Son faible poids aide à réduire la consommation d’énergie, tandis que sa bonne conductivité thermique en fait un matériau idéal pour évacuer la chaleur dans les batteries et les processeurs.
Fluor et énergie
Le fluor joue aussi un rôle clé dans de nombreuses technologies de l’énergie. Historiquement, il est utilisé dans le domaine nucléaire sous forme d’hexafluorure d’uranium (UF6), un gaz dès 60 °C indispensable pour séparer les isotopes de l’uranium et ainsi produire le combustible des réacteurs. Mais son importance ne s’arrête pas là. Outre les PFAS employés comme revêtements de panneaux solaires et de pales d’éolienne pour les protéger des intempéries, le fluor est très présent dans le domaine des énergies renouvelables. Dans ce domaine, le véritable défi ne réside pas dans la production, mais plutôt dans le stockage et la redistribution. En effet, celle-ci est intermittente et est générée que lorsqu’il y a du vent ou du soleil, alors qu’elle doit être disponible à tout moment : quelle serait l’utilité d’allumer la lumière lorsque le soleil brille ? Or, l’électricité n’est rien d’autre qu’un mouvement d’électrons, et un mouvement, par définition, ne se stocke pas. Ce que l’on peut en revanche conserver, ce sont les électrons déplacés, en les piégeant sous une forme chimique ; c’est précisément le rôle des batteries. Dans ce domaine, le fluor intervient à plusieurs niveaux. L’électrolyte des batteries lithium-ion contient un sel fluoré (LiPF₆) qui facilite le transport des ions et des additifs fluorés prolongent la durée de vie de la batterie. Par ailleurs, certains polymères fluorés, en particulier le PVDF (polyfluorure de vinylidène = PFAS), servent de liants pour renforcer la cohésion des électrodes. Enfin, de nouveaux matériaux fluorés inorganiques, comme Na3V2(PO4)F3 – découvert à l’Institut des Molécules et Matériaux du Mans (IMMM) – a ouvert la voie aux batteries sodium-ion, une alternative sans lithium aux batteries actuelles, aujourd’hui commercialisées par la start-up française, Tiamat (Amiens). Une autre façon de stocker l’électricité issue des énergies renouvelables est de le faire sous forme de carburant stockable comme l’hydrogène à l’aide d’un électrolyseur qui sépare, grâce à l’électricité, les molécules d’eau (H₂O) en hydrogène (H2) et en oxygène (O2). Leur fonctionnement repose notamment sur une membrane fluorée capable de laisser passer uniquement les ions tout en bloquant les gaz.
Fluor et avenir
Du nucléaire aux renouvelables, le fluor est omniprésent dans les technologies énergétiques modernes. Il contribue à la production, à la conversion et au stockage de l’énergie, tout en améliorant l’efficacité et la durabilité des dispositifs. Mais quel sera son rôle dans le futur ? L’équipe Cristallochimie d’Oxydes et de Fluorures Inorganiques (COFI) de l’Institut des Molécules et Matériaux du Mans (IMMM) s’attache justement à tirer parti des propriétés uniques du fluor pour concevoir de nouveaux matériaux innovants, capables de répondre aux défis de la transition énergétique.
Le fluor pour les prochaines générations de batteries Li-ion
Le fluor est un atome très particulier : il attire les électrons plus qu’aucun élément du tableau périodique. Cela signifie qu’arracher des électrons à un matériau contenant du fluor demande plus d’énergie que la batterie pourra restituer en temps voulu. Dans le projet CHABLI, financé par la Région Pays de la Loire via le dispositif Etoiles Montantes, nous cherchons à exploiter cette singularité des fluorures pour concevoir de nouveaux matériaux de batteries. L’objectif est de développer des matériaux de batteries à base de métaux abondants, bon marché et non toxiques comme le fer, le manganèse ou le titane, tout aussi, voire plus performants que les matériaux existants contenant du cobalt et du nickel. Cependant, un défi demeure : ces batteries contiennent encore un élément rare, le lithium. Alors, une question se pose naturellement : et si on remplaçait le lithium par le fluor ?
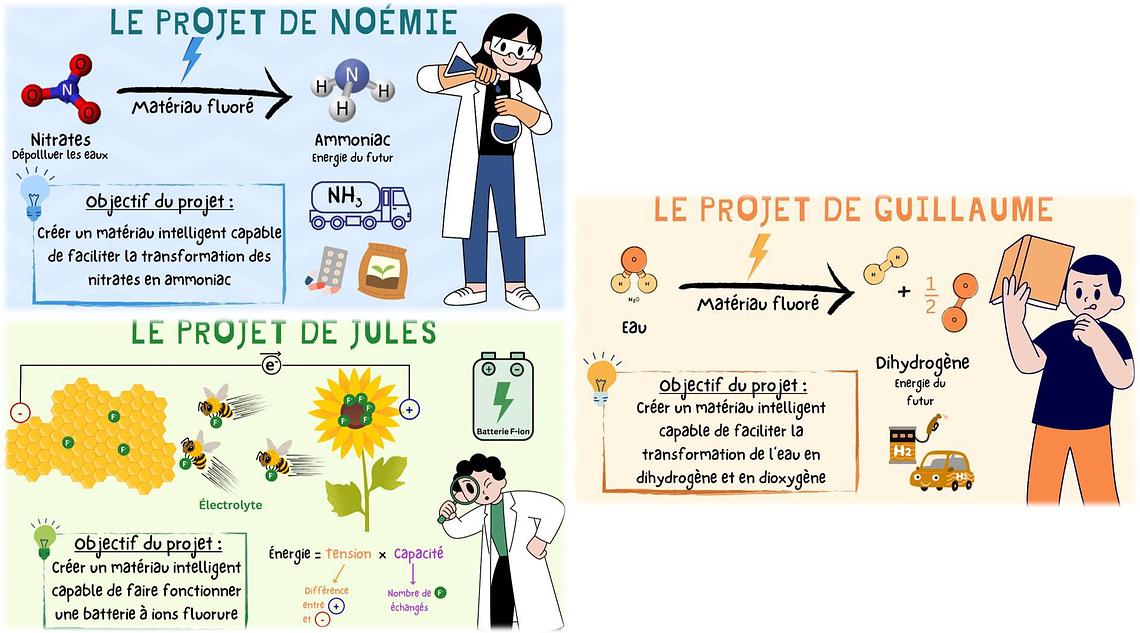
Le fluor, le futur lithium ? Les batteries à ions fluorure (projet de thèse de Jules Valentin)
Dans une batterie lithium-ion, c’est le lithium qui, voyageant entre les deux électrodes, permet le stockage des électrons. Dans une batterie fluor-ion, c’est le fluor qui assure ce rôle. Cette nouvelle technologie de batterie, sans lithium, pourrait permettre de tripler l’autonomie des batteries tout en réduisant leur coût. Le problème, c’est que, pour l’heure, ces batteries révolutionnaires ne peuvent fonctionner que si elles sont chauffées à 150 °C. L’objectif du projet FRISBI, financé par l’état via le plan France 2030, est de développer une batterie fluor-ion qui serait capable de fonctionner à température ambiante.
© Jules Valentin
Le fluor et la production décarbonée d’hydrogène à partir de l’eau (projet de thèse de Guillaume Duval)
La décomposition de l’eau pour produire de l’hydrogène est un procédé aussi ancien que la chimie moderne. En effet, c’est grâce à cette expérience qu’Antoine Lavoisier, en 1783, formula sa célèbre maxime : « rien ne se perd, rien ne se crée, tout se transforme ». À l’époque, il s’agissait d’une découverte purement fondamentale. Aujourd’hui, elle trouve une application très concrète avec la production d’hydrogène comme carburant vert à l’heure où l’hydrogène est encore majoritairement issu de dérivés de pétrole générant d’importantes émissions de CO2. Depuis le début du XIXe siècle, nous sommes capables de produire de l’hydrogène par électrolyse de l’eau grâce à l’électricité mais le problème est que cette réaction n’est pas très efficace. En effet, il faut apporter beaucoup plus d’énergie que celle que l’hydrogène restituera en se recombinant à l’oxygène pour redevenir de l’eau. Pour améliorer le rendement, des matériaux que l’on appelle catalyseurs sont utilisés mais, les plus efficaces actuellement, à base d’oxydes de ruthénium et d’iridium, sont extrêmement coûteux. C’est là qu’intervient une avancée récente de l’équipe COFI : la découverte d’une nouvelle famille de matériaux fluorés, à la fois plus performants, moins chers et bien plus abondants. Le projet MELODHy, soutenu par Le Mans Métropole, vise à optimiser ces catalyseurs prometteurs pour rendre la production d’hydrogène à la fois propre, efficace et accessible, réalisant ainsi la prophétie de Jules Verne : « mes amis, je crois que l’eau sera un jour utilisée comme combustible, que l’hydrogène et l’oxygène qui la constituent fourniront une source de lumière et de chaleur inépuisable ».
© Guillaume Duval
Le fluor pour la dénitrification des eaux couplée à la production d’ammoniac décarbonée (projet de thèse de Noémie Andrieu)
Transformer un produit sans grande valeur, voire nuisible, en une ressource utile fut l’ambition ultime des alchimistes médiévaux qui rêvaient de transformer le plomb en or. Aujourd’hui, nous savons que la chimie en est incapable, mais leur quête a laissé une idée féconde : la valorisation des polluants. Et si, plutôt que de subir la pollution des nitrates (NO₃-), responsables des marées vertes en Bretagne, on les transformait en prometteuse source d’hydrogène, l’ammoniac (NH3), molécule également essentielle à la fabrication de médicaments et d’engrais ? non pas par alchimie, mais par électrochimie ! Le catalyseur est à l’électrochimie ce que la pierre philosophale est à l’alchimie et l’équipe COFI a récemment découvert un composé fluoré extrêmement efficace. L’objectif du projet MOSAR, financé Le Mans Université, est de développer de nouveaux matériaux fluorés capables de promouvoir l’efficacité de cette réaction, afin que l’ammoniac devienne un vecteur énergétique qui aidera à atteindre la neutralité carbone.
© Noémie Andrieu
Si vous souhaitez en savoir davantage sur le fluor et ses multiples facettes, venez discuter avec nous au village des sciences du Mans à l’occasion de la Fête de la Science (les 11 et 12 octobre 2025, à l’Abbaye de l’Epau) sur le stand : Le fluor, un ennemi qui vous veut du bien.
Pour en savoir plus, voici quelques liens utiles:
https://new.societechimiquedef...
https://new.societechimiquedef...
https://new.societechimiquedef...
https://www.cancer-environneme...
https://www.cnrs.fr/fr/actuali...