Les hydrogels : de nouveaux outils pour mieux comprendre et réparer le cartilage
Publié par Nantes Université, le 22 avril 2026 560
Le cartilage est un tissu essentiel au bon fonctionnement des articulations. Cependant, il peut se dégrader au cours de la vie : avec l’âge, l’obésité, certaines pathologies ou à la suite de chocs et de mouvements répétés, il peut s’user progressivement, entraînant des douleurs et une réduction de la mobilité. Aujourd’hui, il n’existe aucun traitement capable de réparer le cartilage. C’est pourquoi la recherche s’attache à comprendre comment reproduire du cartilage en laboratoire, dans l’espoir, un jour, de pouvoir remplacer ou réparer le tissu endommagé.
Le cartilage, un tissu essentiel des articulations…
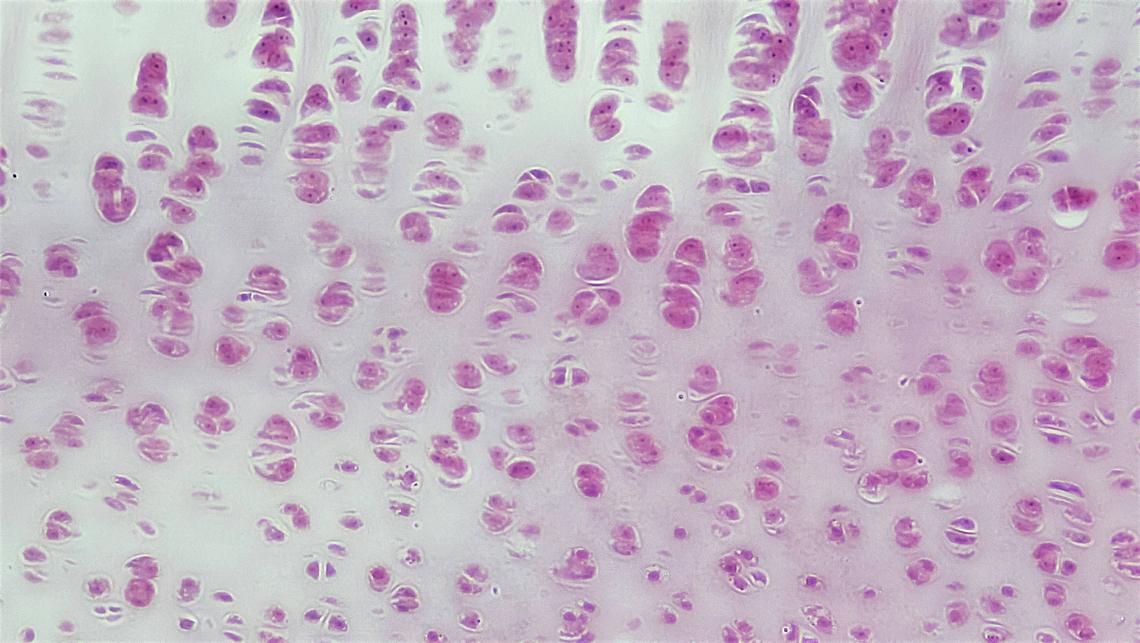
Le cartilage articulaire joue un rôle crucial dans le fonctionnement des articulations. C’est un tissu résistant, à l’apparence lisse, blanche et légèrement transparente, qui recouvre les surfaces osseuses et permet à la fois de réduire les frottements lors des mouvements et d’absorber les chocs en cas d’impact. Il est majoritairement composé d’eau (70 à 80 %), de collagène et d’autres molécules capables de retenir l’eau. Cette substance très hydratée est produite par des cellules spécifiques du cartilage, les chondrocytes, et c’est elle qui confère au cartilage articulaire ses propriétés de lubrifiant et d’amortisseur.
… aux propriétés de régénération très limitées.
Contrairement à d’autres tissus comme la peau ou l’os, le cartilage est dépourvu de vaisseaux sanguins et ne reçoit donc des nutriments que par diffusion : les nutriments traversent progressivement le tissu, depuis sa surface vers les couches plus profondes, de manière lente et limitée. De la même manière, de nouvelles cellules peuvent difficilement être apportées au tissu pour le réparer en cas de lésion, ce qui confère au cartilage des capacités d’auto-renouvellement et de régénération très limitées. De plus, le cartilage articulaire contient peu de cellules, et ses chondrocytes se divisent relativement lentement, ce qui restreint encore davantage sa capacité à se renouveler. Ainsi, lorsque le cartilage est abîmé, que ce soit à la suite d’un choc important, dans le contexte d’une maladie articulaire comme l’arthrose, ou simplement avec le vieillissement, il ne peut pas se régénérer spontanément. Un cartilage endommagé peut alors provoquer des raideurs, des douleurs et une diminution de la mobilité chez les personnes atteintes, pouvant aller jusqu’à un réel handicap. À ce jour, il n’existe aucun traitement permettant de réparer le cartilage, les approches actuelles visant uniquement à soulager la douleur. Il existe donc un réel besoin de mieux comprendre comment réparer ce tissu. L’une des pistes explorées consiste à produire du cartilage « in vitro », c’est-à-dire en dehors d’un organisme vivant, à partir de cellules et de matériaux. Une telle approche permettrait non seulement de mieux étudier le cartilage en laboratoire et d’identifier des molécules susceptibles de favoriser sa régénération, mais aussi, à terme, de produire suffisamment de tissu pour réparer directement le cartilage endommagé.
Comment recréer du cartilage en laboratoire ?
Se pose alors la question : « Comment obtenir du cartilage in vitro ? » Comme évoqué précédemment, le cartilage est constitué d’une substance très hydratée sécrétée par les chondrocytes. Produire du cartilage in vitro implique donc de cultiver ces cellules dans des conditions qui leur permettent de synthétiser efficacement cette substance. Traditionnellement, en laboratoire, les cellules sont cultivées en deux dimensions (2D), généralement sur du plastique traité pour favoriser leur adhésion. Dans ces conditions, les chondrocytes adoptent une morphologie allongée, très différente de la morphologie arrondie qu’ils présentent dans le cartilage articulaire. Ce changement s’explique par le fait que les cellules sont cultivées sur une surface 2D très rigide, un environnement très différent du milieu naturel des chondrocytes. Ce changement de morphologie s’accompagne d’autres altérations des fonctions cellulaires : en culture 2D, les chondrocytes prolifèrent beaucoup plus vite, mais produisent aussi des molécules différentes de celles synthétisées dans le cartilage sain. Ces différences conduisent à la formation d’un tissu cartilagineux de moins bonne qualité, qui peut moins bien résister aux forces de compression.
Les hydrogels : un environnement 3D pour la culture des chondrocytes.
Afin d’obtenir un cartilage de meilleure qualité, il est donc nécessaire d’identifier les conditions de culture qui permettent aux chondrocytes de conserver leurs caractéristiques naturelles. Une approche intéressante pour répondre à ce défi repose sur la culture cellulaire tridimensionnelle dans des hydrogels. Les hydrogels sont constitués de réseaux de polymères hydratés. Un polymère est une longue molécule constituée d’unités répétées, comme le collagène ou l’acide hyaluronique. Mis en solution, ces polymères s’organisent en un réseau capable d’emprisonner l’eau, formant ainsi un hydrogel, comparable à une gelée très hydratée. De manière intéressante, des cellules peuvent être piégées à l’intérieur de ces hydrogels pour être cultivées : on parle alors d’encapsulation. Dans ces conditions, les cellules sont entourées d’un environnement qui reproduit bien mieux les propriétés du cartilage naturel. Mais reproduire cet environnement tridimensionnel a-t-il réellement un effet sur le devenir des chondrocytes ? La réponse est oui. De nombreuses études ont montré que l’encapsulation des chondrocytes dans des hydrogels permettait de mieux préserver leurs fonctions, notamment en favorisant la production d’un tissu dont la composition, l’organisation et les propriétés mécaniques se rapprochent davantage de celles du cartilage articulaire.
Adapter les hydrogels pour mieux cultiver les chondrocytes.
Bien que l’on sache aujourd’hui que les hydrogels permettent d’obtenir du tissu cartilagineux de meilleure qualité, il reste nécessaire d’identifier quelles propriétés des hydrogels favorisent au mieux cette production, afin d’envisager des applications médicales. De manière intéressante, les propriétés mécaniques et biochimiques des hydrogels peuvent être ajustées afin de fournir des signaux différents aux cellules encapsulées. Parmi les propriétés mécaniques, il est par exemple possible d’ajuster la rigidité d’un hydrogel, afin de le rendre plus ou moins dur, un paramètre que les cellules perçoivent et qui influence directement leur comportement. On peut également moduler la viscoélasticité d’un hydrogel, c’est-à-dire sa capacité à se déformer puis à dissiper l’énergie après l’application d’une force (une propriété que l’on retrouve dans le cartilage articulaire). Il est désormais établi que des hydrogels présentant une rigidité intermédiaire, ni trop mous (comme le cerveau), ni trop rigides (comme l’os), sont plus favorables à la culture des chondrocytes. De la même manière, des hydrogels viscoélastiques permettent aux chondrocytes de mieux produire et déposer du tissu cartilagineux que des hydrogels qui ne présentent pas cette propriété.
Quels polymères pour soutenir les chondrocytes ?
Il est également possible de modifier la composition des hydrogels. En particulier, on peut choisir différents types de polymères, tels que le collagène, la gélatine, l’acide hyaluronique, ou encore l’alginate, qui diffèrent par leurs effets sur le comportement des cellules. Par exemple, le collagène et la gélatine favorisent l’adhésion cellulaire. L’acide hyaluronique est, quant à lui, connu pour interagir avec les cellules et moduler certains processus biologiques, comme l’inflammation ou la formation de capillaires sanguins. À l’inverse, certains polymères comme l’alginate sont dits « bio-inertes », ne pouvant pas être reconnus par les cellules et ayant donc, en théorie, un effet neutre sur leur comportement. Cependant, l’influence des différents polymères sur le comportement des chondrocytes au sein des hydrogels reste encore mal comprise, ce qui complique l’identification des conditions optimales pour fabriquer du cartilage in vitro.
Des hydrogels nouvelle génération pour l’ingénierie du cartilage.
C’est dans ce contexte que s’inscrit ce projet de thèse, qui avait pour objectif de concevoir des hydrogels viscoélastiques à base de différents polymères : acide hyaluronique, héparosan et alginate, afin d’identifier quels polymères sont les plus favorables à la culture des chondrocytes. Nos résultats ont montré que les chondrocytes encapsulées dans ces hydrogels étaient capables de retrouver leurs fonctions, quel que soit le polymère utilisé, même après des périodes prolongées de culture 2D les ayant conduits à proliférer et à perdre leur fonction initiale. Nous avons toutefois observé que l’acide hyaluronique et l’héparosan favorisaient plus fortement l’expression de certains gènes liés à la production de tissu cartilagineux que l’alginate. Une autre particularité de ces hydrogels réside dans leur capacité à être dissous à la demande, en seulement quelques minutes, par simple addition d’une petite molécule similaire au glucose. Ces hydrogels permettent ainsi de restaurer les fonctions des chondrocytes après des périodes de culture 2D, mais aussi de les extraire facilement des hydrogels pour mieux les analyser, les faire proliférer à nouveau en 2D ou encore d’envisager leur injection chez le patient. Ce type d’approche ouvre des perspectives intéressantes, notamment pour mieux comprendre les interactions entre les cellules et leur environnement et pour développer des systèmes de culture innovants permettant la prolifération et le maintien des fonctions des chondrocytes. À plus long terme, elle pourrait également contribuer au développement de stratégies visant à produire du cartilage in vitro ou à utiliser ces cellules dans des approches de thérapie cellulaire.
Article rédigé par Garance Saint-Pé, doctorante dans le groupe BIOMAX au laboratoire RMeS (Médecine Régénératrice et Squelette), sous la direction de Vianney Delplace et Claire Vinatier. Les années de thèses sont cofinancées par la Région Pays de la Loire et l’Agence Nationale de la Recherche (projet GELMECS, ANR-22-CE19-0020).